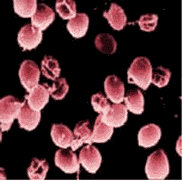
Cryptosporidium parvum
Reservatório: O homem, o gado e animais domésticos.
Modo de transmissão: Fecal-oral, de animais para o
homem ou entre pessoas, pela ingestão de oocistos, que são formas
infecciosas e esporuladas do protozoário.
Período de incubação: De 2 a 14 dias.
Período de transmissibilidade: Várias semanas, a partir do início dos sintomas e enquanto houver eliminação de oocistos nas fezes. Fora do organismo humano, em ambientes úmidos, o oocisto pode permanecer infectante por até seis meses.
Complicações: Enterite, seguida de desnutrição, desidratação e morte fulminante. Comprometimento do trato biliar.
Diagnóstico Laboratorial: Identificação do oocisto do parasito através de exame de fezes. Biopsia intestinal, quando necessária. O diagnóstico também pode ser realizado pela detecção do antígeno nas fezes, através do ensaio imunoenzimático (ELISA) ou através de anticorpo monoclonal marcado com fluoresceína.
Diagnóstico diferencial: Em pacientes com aids, deve ser realizado o diagnóstico diferencial com outros agentes causadores de enterites, como: Giardia lamblia, Entamoeba histolytica, Salmonella, Shigella, Campylobacter jejuni, yersínia, criptosporideos e microsporídeos.
Características epidemiológicas: Ocorre em todos
os continentes. Em países desenvolvidos, a prevalência estimada
é de 1 a 4,5%. Nos países em desenvolvimento, pode atingir até
30%. Os grupos mais atingidos são os menores de 2 anos, pessoas que manipulam
animais, viajantes, homossexuais e contatos íntimos de infectados. Há
relatos de epidemias a partir de água potável contaminada, além
de banhos de piscina ou de lagoas contaminadas.
Objetivo: Não se adota ações de Vigilância Epidemiológica.
Notificação: A criptosporidíase não é uma doença de notificação compulsória.
Medidas de Controle
CARACTERÍSTICAS DO MICRORGANISMO
O Toxoplasma gondii é um protozoário intracelular obrigatório. Os felinos são os únicos "hospedeiros definitivos". O homem e outros animais de sangue quente são "hospedeiros intermediários".
Apresenta três formas infectantes: os taquizoítos (taqui=rápido), que são as formas de proliferação rápida, e estão presentes em grande número, nas infecções agudas. No animal afetado, o parasito pode estar no sangue, excreções e secreções. Neste estágio sobrevive no meio ambiente ou na carcaça por poucas horas. Os bradizoítos (bradi = lento) são formas de reprodução lenta do Toxoplasma gondii, e estão presentes nas infecções congênitas e crônicas. Organizam-se aos milhares em cistos teciduais, particularmente em músculos e tecido nervoso.
Neste estágio pode sobreviver em tecidos por alguns dias depois da morte, mas é destruído pelo congelamento a 12oC por 24 horas ou cocção a 58oC por dez minutos. Os oocistos são as formas resultantes do ciclo sexuado do parasita, que ocorre apenas no trato gastrintestinal dos felídeos. Os oocistos são eliminados nas fezes ainda não esporulados, tornando-se infectantes após a esporulação no meio-ambiente, que ocorre entre 3 e 5 dias de acordo com as condições ambientais. O oocisto esporulado pode permanecer viável no meio ambiente por até um ano e meio (ARAÚJO, 2006).
O Toxoplasma gondii existe em todos os lugares do mundo e infecta a grande maioria dos mamíferos e das aves. Seu ciclo de vida tem duas fases. A primeira é intestinal, só ocorrendo em gatos (selvagens ou domésticos) e produzindo os oocistos. A segunda é extra-intestinal, ocorre em todos os animais infectados (inclusive gatos) e produz taquizoítos, bradizoítos ou zoitocistos que infectam a carne.
Após ingestão pelo gato de tecidos contendo oocistos ou cistos, estes são liberados no organismo e penetram no epitélio intestinal onde sofrem reprodução assexuada seguida de reprodução sexuada se transformando em oocistos, podendo ser excretados junto com as fezes. Oocistos além de poderem sobreviver durante meses no ambiente e são resistentes a desinfetantes, congelamento e processo de secagem, mas destruídos pelo aquecimento a 70ºC por 10 minutos.
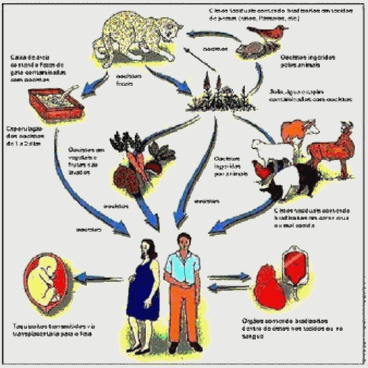
As pesquisas na área da toxoplasmose são de grande importância, por esta doença se constituir uma das zoonoses de maior difusão no mundo em que vivemos.
Pode ser transmitida através de alimentos contaminados por oocistos presentes nas fezes dos gatos ou, mais freqüentemente, por bradizoítos em carne crua ou mal cozida. Na maioria dos humanos infectados a toxoplasmose não produz sintomas.
Entretanto, em determinadas condições, pode resultar em sérias patologias, incluindo hepatite, pneumonia, cegueira e desordens neurológicas severas. Isso é mais verdadeiro para pessoas cujo sistema imunológico esteja muito debilitado, mas também adultos sadios podem produzir sintomas.
O T.gondii, apesar de infectar com freqüência o homem, causa geralmente doença benigna, pois raramente causa distúrbios no seu hospedeiro e, quando isto ocorre, as perturbações são em geral, leves e temporárias. A coriorretinite (acometimento ocular) é a principal forma clínica da toxoplasmose adquirida em indivíduos imunocompetentes.
A toxoplasmose também passa através da placenta, causando aborto espontâneo ou degenerações físicas e mentais no bebê. A distribuição da doença é mundial, e afeta os mamíferos e as aves. A infecção no homem é comum. É mais comum em regiões de clima quente e de baixa altitude. Alta prevalência (85%) de infecção foi relatada na França pelo consumo de carne crua ou mal cozida, enquanto que na América Central a alta prevalência foi relacionada à presença de grandes quantidades de gatos abandonados em climas que favoreciam a sobrevivência de oocistos.
Geralmente assintomática, nos quadros agudos, simulando uma mononucleose, pode apresentar febre, linfoadenopatia, linfocitose e dores musculares que persistem durante dias a semanas. Ocorre transmissão transplacentária, em que o feto apresentará lesão cerebral, deformidades físicas e convulsões desde o nascimento até um pouco depois. Pacientes imunodeficientes são mais acometidos pela infecção, podendo apresentar cerebrite, corioretinite, pneumonia, envolvimento músculo-esquelético generalizado, miocardite, rash maculopapular e/ou morte. Toxoplasmose cerebral é um componente freqüente da AIDS.
Quando a toxoplasmose é no coração, o diagnóstico é dificílimo e geralmente não ocorre a tempo de tratar o paciente. A maioria das confirmações da doença, nesse caso, são feitas pós-morte. Aparece com sintomas de miocardite aguda. Dá ainda arritmias e insuficiência cardíaca.
Caso se instale no cérebro, o Toxoplasma causa encefalite toxoplasmótica, que tem como sintomas principais convulsão e sinais de paralisia. É mais fácil confirmar a doença porque na tomografia aparecem imagens sugestivas.
Os felídeos são o ponto-chave da epidemiologia da toxoplasmose, sendo os únicos hospedeiros da forma sexuada do parasita e, por eliminarem oocistos nas fezes, são a única fonte de infecção dos animais herbívoros. Nestes animais como suínos, caprinos, ovinos, roedores e outros mais, ocorre apenas o ciclo extra-intestinal, com proliferação de taquizoítos nos órgãos e, com a resposta imune, desenvolvem-se os cistos teciduais. Estes permanecem viáveis e são infectantes para os gatos e para os outros hospedeiros intermediários como o homem e o cão. Nestes últimos, a infecção geralmente pode acontecer pela ingestão de oocistos, presentes no solo ou alimentos de origem vegetal, ou de carne com cistos tissulares.
Atualmente, estima-se que um terço da população mundial esteja infectada por toxoplasma. O Brasil apresenta índices que se encontram entre os mais altos descritos, onde inquéritos sorológicos registrados demonstraram uma prevalência variando de 37 a 91%. Entre novembro de 2001 e janeiro de 2002, o Brasil registrou o maior surto de toxoplasmose do mundo, ocorrido no município de Santa Isabel do Ivaí Paraná. Um total de 462 pessoas apresentou sorologia sugestiva para toxoplasmose (IgM reagente). Dentre os acometidos, 07 eram gestantes e destas, 06 tiveram seus filhos infectados, ocorrendo uma anomalia congênita grave e um aborto espontâneo. A investigação epidemiológica concluiu que a fonte de contaminação era um dos reservatórios de água da cidade que estava contaminado por fezes de um gato que estava eliminando oocistos de toxoplasma.
No dia 08 de fevereiro de 2006, a Secretaria de Vigilância em Saúde do Ministério da Saúde SVS/MS foi notificada pela Secretaria Estadual de Saúde de Goiás SES/GO sobre a ocorrência de um surto de toxoplasmose no município de Goiânia/GO. As informações preliminares repassadas pela Vigilância Sanitária Municipal (órgão que recebeu a denúncia) eram de que seriam 11 casos de toxoplasmose confirmados por resultados laboratoriais.
Essas pessoas haviam participado de uma festa de confraternização de natal em um restaurante de Goiânia, realizada no dia 17 de dezembro de 2005. Nesta festa estiveram presentes 26 pessoas (incluindo os casos já confirmados). O alimento suspeito foi comprado em uma casa de carnes em Goiânia. Esse estabelecimento vendeu o mesmo alimento para uma festa em Anápolis, onde também houve um surto de toxoplasmose no mesmo período.
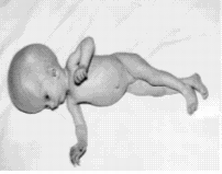
Hidrocefalia
É uma infecção causada por um parasita intracelular, o protozoário Toxoplasma gondii. A toxoplasmose pode ser congênita ou adquirida. Em adultos é assintomática em 80% a 90% dos casos. No entanto, quando a mulher adquire a infecção durante a gestação a doença pode ser transmitida ao feto, que é bastante sensível ao protozoário. A severidade da infecção fetal é mais pronunciada quando a infecção materna é adquirida durante o primeiro trimestre.
A transmissão congênita do T. gondii pode ocorrer quando a infecção aguda coincide com a gravidez, com conseqüências mais sérias aos fetos, no primeiro terço ou metade da gestação, embora quanto mais adiantada a gestação, maior é a probabilidade da infecção fetal, porém com menos riscos de fetopatias graves. O Toxoplasma gondii multiplica-se na placenta e, então difundem-se para os tecidos fetais. Embora a infecção possa se desenvolver durante qualquer estágio da gestação, o feto é afetado mais severamente quando a fêmea gestante se infecta durante a primeira metade da gestação.
As manifestações da TC são variáveis, dependendo muito do momento da gestação (idade gestacional) no qual a mãe foi infectada. A infecção envolve principalmente o sistema nervoso e os tecidos muscular e conjuntivo. Dentre os principais sinais e sintomas destacam-se calcificações intracranianas, alterações no SNC, microcefalia, hemiplegia, tonicidade muscular anormal e coriorretinite ativa (seqüela mais comum, sendo que o risco de novas complicações na retina permanece por alguns anos). Em média, 10 a 15% das crianças infectadas durante a gestação apresentam sintomas neonatais (desenvolvem infecção generalizada).
Nos demais casos as crianças infectadas parecem saudáveis ao nascer, mas podem desenvolver coriorretinites ou sintomas neurológicos mais tardiamente. Seqüelas a longo prazo podem incluir retardo mental, paralisia cerebral, convulsões, surdez e cegueira.
O diagnóstico pré-natal de infecção fetal em gestantes com infecção primária por Toxoplasma gondii pode ser feito por análise do líquido amniótico, vilosidades coriônicas ou amostras de sangue fetal, pesquisando-se a presença do DNA do parasita, pelo isolamento do parasita ou pela identificação dos anticorpos específicos das classes IgM e IgA. Exames de ultrassom de alta resolução podem ser úteis na identificação de manifestações severas no feto.
Aproximadamente em 40% dos casos de mães infectadas, o bebê também é infectado. Cerca de um terço dos bebês com toxoplasmose congênita apresentam problemas detectados por ultra-som.
Cerca de 4.100 das 4,1 milhões de crianças nascidas nos E.U.A. todo ano, com até 50% de infecção transplacentária sendo que a maioria não mostra sinais clínicos ao nascer, mas apresentam alguma seqüela no decorrer da vida. Muitas destas crianças podem desenvolver coriorretinite durante a adolescência ou na fase adulta. No Brasil no mínimo 6 mil bebês nascem por ano com infecção congênita, que é evitável com orientação dietética e acompanhamento sorológico Na região metropolitana de São Paulo, estima-se que devam nascer cerca de 230 a 300 crianças infectadas por ano. Na França e Áustria a incidência de toxoplasmose congênita é de 3-4 casos por cada 1000 nascimentos e no Reino Unido foram descritos 91 casos entre 1975 e 1980.
A transmissão transplacentária ou congênita foi a primeira a ser conhecida como causadora das lesões em humanos. As maneiras mais comuns de contágio são o consumo de alimentos contaminados e o contato com fezes de gato e terra. A importância da toxoplasmose congênita como causa da toxoplasmose ocular passa a ser reconhecida a partir dos trabalhos de Wilder 1952(1) e Perkins 1973(2). Setenta por cento das infecções congênitas terão cicatrizes retinocoroideanas.
Um dos problemas mais diagnosticados é a hidrocefalia que corresponde ao acúmulo de fluído nos ventrículos cerebrais, portanto Hidrocefalia Pré-natal que pode ser severa a ponto de impedir parto normal.
A toxoplasmose pode levar à cegueira. Se o parasita não atingir a mácula (centro) da retina, os prejuízos para a visão são menores. Gera uma visão turva, mas o paciente voltar a ver normalmente depois do tratamento. Se atingir a mácula, a pessoa perde a visão central e fica apenas com a periférica. A terapêutica é feita com medicamentos orais fortes, compostos de sulfas e pirimetamina.
A toxoplasmose ocular é a causa mais comum de inflamação retiniana em pacientes imunocompetentes e uma das mais importantes infecções oculares secundárias em pacientes com AIDS.
Abreu et al. 1998(11), realizaram um estudo populacional para conhecer a prevalência da toxoplasmose ocular em Venda Nova do Imigrante, ES, e compará-la com a prevalência de lesões em outras regiões do Brasil. De 1074 pessoas examinadas, 11,27% foram diagnosticadas como portadoras da toxoplasmose ocular, baseado em achados fundoscópicos. Esta prevalência foi superior à existente nos Estados Unidos (0,6%) e em São Paulo (9%), mas inferior à de Erechim, RS (17,7%).
Cerca de 70% da população adulta das cidades já se infectaram com o protozoário Toxoplasma gondii, que causa a Toxoplasmose, doença resultante da ingestão de alimentos crus, mal cozidos ou do contato com fezes de gatos.
No Ceará, dos 1.133 exames realizados no ano passado pelo Laboratório Central de Saúde Pública (Lacen), apenas 19 deram positivos - um percentual de 1,67%. Conforme a bioquímica do Lacen, Lúcia Roriz, a maioria das pessoas que realiza o exame está grávida ou apresenta problemas de visão.
Estudioso da doença há 25 anos, o infectologista Ivo Castelo Branco explica que, na maioria dos casos, não há sintomas. Quando os sinais da doença se manifestam, eles podem ser confundidos com o de uma virose ou mesmo dengue (febre, dor no corpo,...). A toxoplasmose tem cura e o tratamento leva em torno de um a seis meses.
Dr. Ivo Castelo Branco informa que o Brasil nunca teve epidemia da doença. Ao ingerir o alimento contaminado, o protozoário se instala em qualquer órgão do corpo humano. Em alguns pacientes pode atingir os olhos e levar à cegueira, ou mesmo acarretar cistos cerebrais, só diagnosticados com ultra-sonografia. A grande maioria dos pacientes que atende em seu consultório comeu alimentos crus ou carne mal passada. Alguns tinham por hábito degustar sushi (comida japonesa à base de peixe cru). Contudo não se sabe se isso é apenas uma coincidência.
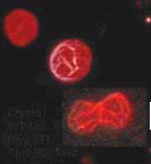
Toxoplasma gondii
Reservatório: os hospedeiro definitivos de Toxoplasma gondii são os gatos e outros felinos que se contaminam pela ingestão de mamíferos.
Modo de transmissão: O Toxoplasma gondii é transmitido ao homem por diversas maneiras: através da ingestão de carne mal cozida contendo cistos de Toxoplasma; pela ingestão de oocistos provenientes de mão contaminada por fezes ou alimento e água; transmissão transplacentária; inoculação acidental de traquizoítos ou pela ingestão de oocistos infectantes na água ou alimento contaminado com fezes de gato. Pode ocorrer transmissão através da inalação de oocistos esporulados. As fezes de cabras e vacas infectadas podem conter traquizoítos. A infecção por transfusão de sangue e transplante de órgãos de um doador infectado é rara, porém pode ocorrer.
Período de incubação: consiste de 10 a 23 dias quando a infecção provém da ingestão de carne mal cozida; de 5 a 20 dias em uma infecção associada a gatos.
Complicações: Caso se instale no cérebro, o Toxoplasma causa encefalite toxoplasmótica, que tem como sintomas principais convulsão e sinais de paralisia. Durante o primeiro trimestre de gestação, pode causar deformidades no feto. Em casos mais graves de toxoplasmose ocular, pode levar a cegueira.
Susceptibilidade e resistência: todos estão susceptíveis à infecção, porém a imunidade é facilmente adquirida e muitas infecções são assintomáticas. Os pacientes que são tratados por citotóxicos ou imunossupressores são mais susceptíveis à infecção.
Diagnóstico laboratorial: o diagnóstico se baseia nos sinais clínicos e pela confirmação através de estudos sorológicos, pela demonstração do agente em tecidos ou líquidos corporais pela biópsia ou necrópsia ou pela identificação do agente em animais ou através do cultivo de material. Aumentos dos níveis de anticorpos apontam para infecção ativa. A presença de IgM específico e/ou aumento dos títulos de IgG em soro seqüencial de crianças é evidencia conclusiva de infecção congênita. Altos níveis de anticorpos IgG podem persistir por anos não significando atividade da doença. Pode-se detectar material genético do parasita por técnicas de biologia molecular, principalmente nas infecções congênitas no útero.
Tratamento: o tratamento não é necessário para pessoas saudáveis e que não estejam grávidas. Para mulheres grávidas e pessoas com deficiência do sistema imunológico, o tratamento deve ser feito com pirimetamina, sulfadiaziana e ácido fólico durante quatro semanas. Clindamicina em adição a esses agentes é utilizada para tratamento da toxoplasmose ocular. Espiramicina é usada em gestantes para prevenir a infecção placentária.
Medidas de controle
Pesquisa de Antígeno p24: este teste quantifica concentração da proteína do core viral p24 presente no plasma ou no sobrenadante de cultura de tecido. Embora esta proteína esteja presente no plasma de pacientes em todos os estágios da infecção pelo HIV, sua maior prevalência ocorre antes da soroconversão e nas fases mais avançadas da doença, o teste é feito utilizando-se a técnica de ELISA (imunoenzimático).
Entre os métodos diretos, a identificação
do parasita pode ser realizada em esfregaços de secreção
ocular corados pela técnica de Giemsa, em que se pesquisa a presença
dos taquizoítos, com sua característica forma em meia-lua. O exame
citológico pelo método de Giemsa também é
útil em material de biópsia, principalmente punções
de linfonodo e fígado, assim como nos lavados traqueobrônquicos,
principalmente nos gatos. O exame histopatológico é limitado,
uma vez que nos cortes teciduais o parasita se confunde com as células
do hospedeiro. Neste caso é indicada a utilização de técnicas
de imunohistoquímica, como a da peroxidase-anti-peroxidase e da
streptavidina-peroxidase, que identificam de forma muito sensível
e específica, os microrganismos nas lesões.
ARAÚJO, W.N.; SILVA, Aristeu V.; LANGONI, Hélio. Toxoplasmose: uma Zoonose - Realidades e Riscos. 2004.
BENENSON, AS. El Control de las enfermidades transmisibles em el hombre. 15º ed. Washington, DC: Informe oficial de la Asociación Estadounidense de Salud Pública,1992: 652 520.
BIREME. Disponível em: http://www.bireme.br/ acesso dia 20/06/2006
CDC/ATLANTA/USA. DPDx - Toxoplasmosis. In: www.dpd.cdc.gov/dpdx 2006.
CHAPPELL, CL et al. Cryptosporidim parvum: intensity of infection and oocysts excretion patterns healthy volunterrs. Lounal of Infect Dis, v 173, n1, p 232-36, Jan 1996.
CHIEFFI, PP et al. Infection by Cryptosporidium parvum I renal patients submitted to renal transplant or hemodialysis. Rev. Soc. Bras. Méd. Trop., v31, n4, p333-37, Jul/Aug 1998.
COSTA, Danilo Pereira; ACHÊ, Paulo Nicolau Ferreira. Criptosporidiose. Faculdade de Medicina da Universidade de Ribeirão Preto UNAERP, 2006.
DIÁRIO DO NORDESTE. TOXOPLASMOSE: DOENÇA DO GATO. (11/6/2006).
Dubey JP, and Beattie CP. Toxoplasmosis of animals and Man. CRC Press, Baca Raton, Florida, 52, 1988.)
FAYER, R et al. Epidemiology of Cryptosporidium: transmission, detection and identification. Internacional Journal for Parasitology. v. 30, p 1305-22, 2000.
FERNANDES, Antonio Tadeu. Patógenos hospitalares emergentes: Cryptosporidium, E. coli O157:H7, Helicobacter pylori e hepatite C: epidemiologia, sobrevivência no meio ambiente, eficácia da desinfecção e medidas de controle. In
FRANCO, RM et al. Occurrence of Cryptosporidium Oocysts and Giardia cysts in raw water from the Atibaia River, Campinas, Brazil. Ver. Inst. Med. Trop., v 43, n 2, Mar/Apr 2001.
FRANZEN, C; MULLER, A. Cryptosporidia and Microspodidia Waterborne diseases in the Immunocompromised Host. Diagn Microbiol Infect dis., v 34, p 245-62, 1999.
Guia Brasileiro de Vigilância Epidemiológica 1998. 1998. Ministério da Saúde. Fundação Nacional de Saúde.
HIRAMOTO, Roberto Mitsuyoshi; GALISTEO, Andrés Jimenez Jr. TOXOPLASMOSE. IMT - Instituto de Medicina Tropical de São Paulo / USP - Laboratório de Protozoologia. IPEN - Instituto de Pesquisas Energéticas e Nucleares / USP - Laboratório de Biologia Molecular.
INFORME-NET DTA. Secretaria de Estado da Saúde de São Paulo. Centro de Vigilância Epidemiológica - CVE. MANUAL DAS DOENÇAS TRANSMITIDAS POR ALIMENTOS. TOXOPLASMA GONDII/TOXOPLASMOSE.
LABERGE, I; GRIFFITHS, MW. Prevalence, detection and control of Cryptosporidium parvum in food. Int. J. Food. Microb., v 31, p 1 26, 1996.
LEAL, Diego AG; PEREIRA, Mirna A.; FRANCO, Regina MB; BRANCO, Nilson. Padronização de uma Técnica para Detecção de Oocistos de Cryptosporidium spp. em Moluscos Bivalves usualmente Ingeridos Crus. UNICAMP. Jun/jul de 2005.
MALTEZ, Danilo de Souza. Divisão de Doenças de Transmissão Hídrica e Alimentar. Faculdade Metodista, 2002.
MARTINS, CAP; GUERRANT, RL. Cryptosporidium and Cryptosporidiosis. Parasitology today. V 11, n 11, 1995.
SCAGLIA, M et al. Cryptosporidium parvum life cycle in cuckling mice: a Normarski interference-contrat study of a human-derived strain. J. Protozool. V38, n6, p 1185-1215. Nov/Dec, 1991.
SCHNEIDER, MME.charge in natural history of opportunistic infections in Hiv-infected patients. The Netherlands Journal of Medicine. v57, n 1-3, 2000.
SILLOS, Marcela Duarte; FACUNDES, Ulysses Neto. FOODBORNE - Doenças Veiculadas por Alimentos. 2002.
SILVEIRA, Cláudio. Toxoplasmose - Levantamento bibliográfico de 1997 a 2000.
TAVARES, Tatiana; ARAÚJO, Ana Júlia US; UENO, Mariko. Ocorrência de Cryptosporidium spp em Alfaces (Lactuca sativa) Servidas em Restaurantes "Self-Services" da Cidade de Taubaté-SP. Universidade de Taubaté, Set/2004 Mar/2005.
WEBER DJ, RUTALA WA. The emerging nosocomial pathogens Cryptosporidium, Escherichia coli O157:H7, Helicobacter pylori, and hepatits C: epidemiology, environmental survival, efficacy of desinfection, and control measures. Infect Control Hosp Epidemiol, 2001(22) 5:306-315.
Mª Aliciane Fontenele Domingues
Mestranda em Tecnologia de Alimentos, Universidade Federal do Ceará UFC.
aliciane_fontenele[arroba]yahoo.com.br
|
|
|