 Página anterior Página anterior |   Voltar ao início do trabalho Voltar ao início do trabalho | Página seguinte  |
Analisador Elementar
No sistema automatizado, o processo analítico elementar é intermediado por um sistema de combustão e um de redução. O sistema de combustão é composto por um tubo de quartzo preenchido, em um forno à 1000 °C, com um catalisador Cr2O3 e CuO em fios cortados em pequenos pedaços, que tem por objetivo oxidar hidrocarbonetos e lã de prata, que tem a função de reter o enxofre (SO2) e ainda halogênios1. Os produtos da combustão, auxiliados por um pulso de O2, tanto para amostras sólidas como líquidas, constituídos principalmente de CO2, N2, NOx e H2O são conduzidos (com fluxo de He) para o sistema de redução, também composto por um tubo de quartzo, num forno à 600 °C, contendo cobre metálico (Cuo). Nesse sistema, os óxidos de nitrogênio são reduzidos à N2, sendo também retido o excesso de O2 utilizado na combustão da amostra. Nesse processo ocorre a oxidação do cobre (Cu+2), formando óxido de cobre (CuO) no forno de redução. A reação de combustão da amostra e oxidação do cobre metálico podem ser verificadas nas equações (1) e (2).
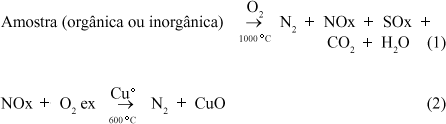
onde: O2 ex = Oxigênio em excesso na reação de combustão da amostra; SOx (óxidos de enxofre) são retidos no forno de combustão contendo Ag; H2O retida em coluna de Mg(ClO4)2 e CO2 retido (nas determinações isotópicas de nitrogênio) em coluna de carbosorb (base).
Oxidação do Cobre Metálico
O cobre metálico utilizado no sistema de redução do ANCA-SL 20/20 (Europa Scientific, UK) foi o de referência B1083, com dimensões de 4 x 0,5 mm, acondicionado em ampolas contento 152 g de Cuo.
O óxido de cobre residual, foi obtido do forno de redução do analisador elementar, após oxidação de aproximadamente 90 % da massa de cobre reduzido adicionado inicialmente. O momento da retirada do cobre oxidado do tubo de redução é dado pelo aparecimento do pico de massa 30, referente ao NO, no espectro de massas apresentado na programação do reprocessador ou por avaliação visual da coluna de redução. Com a saturação da coluna de cobre reduzido, os óxidos de nitrogênio (principalmente NO) não são mais convertidos a N2 (equação 2) no forno de redução. Dessa maneira, os gases N2 e NO são separados no cromatógrafo gasoso (GC), interferindo na mesma massa 30 do espectro. Esse fato causa um fracionamento isotópico, assim como diferenças no teor de N das amostras, resultando em erros analíticos.
Linha de Recuperação do Cobre Metálico (Cuo)
Após o processo de oxidação do cobre metálico, o tubo de quartzo é retirado do interior do forno de redução e o óxido de cobre pesado e posteriormente peneirado com 0,5 e 0,149 mm de crivo, respectivamente. A massa de óxido de cobre que passa pelas duas peneiras (MP) é descartada (depósito de resíduos sólidos) devido à reduzida granulometria. O óxido de cobre que fica retido nas peneiras (MR) é levado à linha de alto vácuo para recuperação do cobre metálico reduzido (Cuo), sob fluxo de H2 à temperatura de 450 °C, conforme observado na Figura 1.

Inicialmente, o óxido de cobre (CuO) é transferido para um tubo de vidro (borosilicato ¾ diâmetro de 18mm) em formato de U, como pode ser observado na Figura 2A. Na seqüência, o tubo em U é introduzido no interior do forno (F1), por um orifício central medindo 25 mm de diâmetro. Após a evacuação do sistema (0,1 mmHg) e a temperatura no interior do forno atingir cerca de 450 °C, é iniciada a passagem de H2 pelo sistema de vácuo. O H2, obtido de um cilindro de 9m3 (gás comercial), é transferido para um balão especial de latex (aproximadamente 2 L).

O H2, em contato com o óxido de cobre à temperatura de 450 °C, dá origem à formação de água, reduzindo o cobre à forma metálica (Cuo). O volume de H2 utilizado em cada batelada é função da quantidade de óxido de cobre utilizado, bem como do estado oxidativo do mesmo (mistura de CuO + Cuo).
A água produzida na reação (MH2O) é retida em uma armadilha de gelo seco e etanol (CO2(s) + C2H5OH), à temperatura de aproximadamente ¾73 °C, conforme observado na linha de alto vácuo. Por segurança, uma segunda armadilha criogênica contendo nitrogênio líquido (-196 °C) é conectada na seqüência da linha de vácuo. A reação é realizada com bombeamento constante utilizando-se uma bomba mecânica de vácuo, protegida por uma armadilha de nitrogênio líquido.
Ao término do processo de redução do cobre, o sistema de aquecimento do forno é desligado e após atingir a temperatura ambiente, é introduzida uma atmosfera inerte de nitrogênio ou argônio no interior do tubo contendo cobre metálico (Figura 2B). Tal procedimento é realizado com o objetivo de evitar uma possível oxidação do cobre metálico. A seguir, o cobre metálico é transferido para um tubo de vidro de borossilicato (280 x 26 mm), previamente pesado, sendo na seqüência determinada a massa do metal (MCuo). Finalmente, o tubo contendo o cobre metálico é levado à linha de vácuo, onde procede-se a evacuação da atmosfera contendo O2 e é introduzido nitrogênio gasoso no interior do tubo, sendo lacrado com maçarico, completando o 1o ciclo de recuperação do cobre.
Após a utilização do cobre (obtido no 1o ciclo) no analisador elementar e posterior oxidação, o mesmo procedimento de redução é efetuado (2o ciclo). No presente trabalho foram efetuados testes de recuperação até o 3o ciclo de reutilização.
O número de determinações isotópicas de 15N ou 13C em amostras sólidas (plantas, solos, celulose, entre outros) ou líquidas (soluções padrão, fertilizantes marcados isotopicamente, vinagre, vinho e derivados, entre outros), possíveis de serem realizados em cada ciclo (carga de cobre metálico utilizado no tubo de quartzo), foram quantificados.
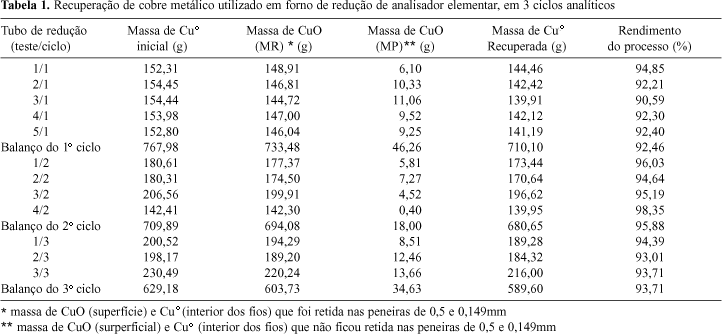
No presente trabalho procurou-se avaliar a recuperação do cobre metálico oxidado originado no processo analítico da determinação elementar e isotópica de C e N usando o ANCA-SL 20/20, durante três ciclos (redução-oxidação). A massa de cobre metálico utilizada incialmente foi de 767,98 g. Essa quantidade de cobre reduzido foi dividida em 5 parcelas no tubo de redução do analisador elementar. A Tabela 1 mostra a quantidade de cobre metálico utilizado em cada teste no 1o, 2o e 3o ciclo, bem como a massa de cobre oxidada (MR), a quantidade de cobre descartado (MP) e o cobre metálico recuperado. A partir desses dados foi possível obter o porcentual de recuperação em cada ciclo das análises. A massa de óxido de cobre, denominada de CuO (MR), representa a massa total obtida após saturação de 90% da superfície do cobre. A massa MR representa o cobre oxidado principalmente na superfície do metal, bem como a massa de cobre metálico que permanece sem oxidação na parte interna dos fios de cobre. A massa MP corresponde à massa de cobre (CuO e Cuo) descartada no processo, devido a sua granulometria (partículas finas, que passam na peneira de 0,149 mm).
No processo de redução do cobre, relacionados com o 1o ciclo, foi obtido cerca de 26 g de água decorrente da reação de oxidação-redução (CuO + H2 ® Cuo + H2O), em todo o ciclo. Esses dados mostram que cerca de 92 gramas do cobre metálico inicialmente empregado foram oxidados a CuO (oxidação superficial), que representou aproximadamente 12% da massa total do cobre inicialmente utilizado.
Avaliando os resultados apresentados na Tabela 1, observou-se que o rendimento do processo de recuperação de cobre Cuo, após completado o 1o ciclo, foi em média de 92,46%. Em tal etapa, foram realizadas determinações isotópicas de nitrogênio e carbono em cerca de 1300 amostras de solo e planta (1,7 amostra por grama de Cuo). A perda de cobre com relação à massa utilizada inicialmente foi da ordem de 58 g, representando 7,54 % da massa empregada inicialmente (767,98 g). Tal perda está principalmente associada com o processo de separação nas peneiras.
Na Tabela 1, pode-se ainda observar os dados com relação ao 2o ciclo do processo de oxidação-redução do cobre, onde foi utilizado 709,89 g de cobre metálico, recuperado no 1o ciclo, sendo essa massa dividida em 4 tubos de quartzo para posterior emprego no processo analítico. No último teste dessa etapa (4/2), ocorreu um problema no espectrômetro de massas (vazamento) e o tubo de redução contendo 142,41 g de cobre foi retirado muito antes da saturação, sendo a perda de cobre insignificante nessa etapa do ciclo. No 2o ciclo foram realizadas determinações isotópicas de nitrogênio e carbono em aproximadamente 900 amostras (1,6 amostra por grama de Cuo), não considerando a última etapa do teste.
Os resultados observados na Tabela 1, mostram que o rendimento médio no processo de recuperação do cobre Cuo, no 2o ciclo, foi da ordem de 95,88%. Nesse ciclo a perda total de cobre foi de aproximadamente 29,24 g, correspondendo a 4,12% da massa inicial (709,89 g) utilizada.
Do total de cobre metálico recuperado no 2o ciclo (709,89 g), foi utilizado 629,18 g para a realização do 3o ciclo. A Tabela 1 apresenta os resultados referentes ao processo de oxidação-redução, empregando três tubos de redução para os testes (1/3, 2/3 e 3/3). No 3o ciclo foi possível recuperar, em média, aproximadamente 93,71% do cobre utilizado no tubo de redução e as perdas totalizaram cerca de 39,58 g ou 6,3% do total inicial empregado. No 3o ciclo, dessa forma, foi possível a determinação isotópica de 860 amostras de planta e solo, correspondendo a 1,4 amostra por grama de Cuo.
Com os resultados obtidos, foi possível calcular as perdas de cobre em cada ciclo como sendo de 5,98 ± 0,99% em relação ao montante inicial utilizado em cada um dos ciclos. Os resultados obtidos após a realização dos três ciclos de recuperação do cobre metálico mostram que, partindo de uma massa de cobre de aproximadamente 760 g, é possível completar cerca de 25 ciclos de oxidação-redução, restando ainda massa suficiente para completar um tubo de redução (150 ¾ 180 g), indicando assim uma projeção analítica em cerca de 8000 amostras para as espécies nitrogênio e carbono.
O sistema de recuperação de cobre em sua forma metálica Cuo empregando hidrogênio como redutor em linha de alto vácuo mostrou ser de elevada eficiência e baixo custo, considerando que o cobre é um dos itens que eleva o preço das determinações elementares e isotópicas (preço internacional de US$ 35,00 por determinação isotópica).
Com a utilização do sistema proposto é possível analisar cerca de 8000 amostras, a partir de um lote inicial de 760 g de cobre metálico Cuo, enquanto que, sem o processo de recuperação, somente cerca de 1200 amostras poderiam ser analisadas. Outro fator importante é a significativa diminuição do rejeito de cobre para disposição final.
Os autores agradecem à Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP) e à Financiadora de Estudos e Projetos (FINEP) pelo apoio financeiro.
1. Barrie, A.; Prosser, S.J. Em Mass Spectrometry of Soils; Boutton, T.W.; Yamsahi, S., ed.; Marcel Dekker: New York, 1996, p. 1.
2. Jardim, W.F.; Quim. Nova 1998, 21, 671.
3. Tuono, V.; Dissertação de Mestrado, Universidade de São Paulo, Brasil, 1999.
4. Lau, L.D.; Rodrigues, R. Henery, S.; Manuel, D.; Schwendiaman, L.; Environ. Sci. Technol. 1988, 32, 670.
5. Brasil, R.B.; Batista, D.; Cardoso, A J.; Nogami, E.M.; Nozaki, J.; Resumos da 20ª Reunião Anual da Sociedade Brasileira de Química, Poços de Caldas, Brasil, 1997.
6. Martin, S.B.; Dougherty, D.J.; Allen, H.E.; Emerging Technol. Hazard. Waste Manage, 1996, p.159.
7. Fleet, B.; Small, C.E.; Jorge, J.; Cazares, S. D.; Asher, R.K.; Bull. Eletrochem. 1993, 539.
8. Cantarow, A.; Schepartz, B. Em Bioquímica; Ateneu, A. Ed.: Rio de Janeiro, 1969, p.12.
9. Bragança, M.J.C.S.; Dissertação de Mestrado, Pontifícia Universidade Católica do Rio de Janeiro, Brasil, 1992.
10. Sunda, W.; Guillard, R.R.L.; J. Marine Res. 1976, 34, 511.
11. Jardim, W.F.; Koning, A.; Pearson, H.W.; Quim. Nova 1984, 7, 138.
12. Schmidt, R.L.; Environ. Control. 1978, 8, 247.
13. Florence, T.M.; Talanta Review 1982, 29, 345.
José Albertino Bendassolli, Jefferson Mortatti, Paulo Cesar Ocheuze Trivelin, Raquel de Fátima Ignoto, José Aurélio Bonassi e Glauco Arnold Tavares
pcotrive[arroba]cena.usp.br
Centro de Energia Nuclear na Agricultura, Universidade de São Paulo, CP 96, 13400-970 Piracicaba - SP
 Página anterior Página anterior |   Voltar ao início do trabalho Voltar ao início do trabalho | Página seguinte  |
|
|
|